El neutrino es sin duda la partícula más misteriosa del Modelo Estándar. Interacciona tan débilmente con el resto de partículas que resulta realmente muy difícil de detectar, lo que ha hecho que en la actualidad sigamos intentando averiguar muchas de sus propiedades. En este artículo hablaremos de los problemas experimentales que dieron lugar a que se postulara su existencia. Veremos que, como es habitual en ciencia, no siempre se da con la solución correcta a la primera.
Nuestro relato comienza con el descubrimiento de la radiactividad por Henri Becquerel en 1896, una historia de serendipia que merece ser contada en otra ocasión. En resumen, lo que Becquerel descubrió es que algunas sustancias emitían de forma espontánea cierta radiación. Esta observación pronto se convirtió en asunto de gran interés para la comunidad científica de la época y muchos otros investigadores, con Marie y Pierre Curie a la cabeza, comenzaron inmediatamente a investigar las propiedades de dicha radiación. Muy rápidamente se vio que podía ser de varios tipos, siendo el más importante para nuestra narración la llamada radiactividad beta (β). Esta radiación, producida por sustancias que emitían de forma natural electrones, escondía los secretos que motivaron la predicción del neutrino.
Antes de seguir con nuestro relato detengámonos un momento y hablemos sobre la interpretación que se daba a la radiación beta a principios de siglo XX. La observación experimental indicaba dos hechos bien claros: (1) que este tipo de radiactividad cambiaba la composición química de la sustancia que la emitía, y (2) que estaba compuesta por electrones, algo que el propio Becquerel determinó al medir el cociente masa/carga de la radiación. Por lo tanto, era razonable imaginar un átomo como Z electrones situados alrededor de un núcleo, que a su vez está formado por A protones y A-Z electrones (os recordamos que Z es el número atómico y A el número másico). De ese modo el átomo sería eléctricamente neutro y los electrones que componían la radiación beta estarían surgiendo de su núcleo, siendo la radiación beta equivalente a la transición nuclear
(A,Z) → (A,Z+1) + e–
Hoy en día sabemos que esta imagen del átomo estaba equivocada. De hecho, pronto se encontraron dos problemas que no podían entenderse dentro de este modelo.
Una de las primeras cuestiones que se planteó tras el descubrimiento de la radiación beta es qué energía tenían los electrones que la componían. Tras los trabajos iniciales de Otto Hahn y Lise Meitner, el primer gran paso en esta dirección lo dio James Chadwick en 1914. Por aquella época, Chadwick trabajaba en Berlín bajo la supervisión de Hans Geiger, por lo que resultó natural que decidiera utilizar sus famosos contadores para medir con precisión la energía de los electrones emitidos, siendo capaz de mostrar que en lugar de tener una energía fija (como sí ocurría con las radiaciones alfa y gamma), ésta presentaba una distribución continua en la que los electrones podían tener cualquier energía entre 0 y un valor máximo, tal y como se muestra en la siguiente figura.
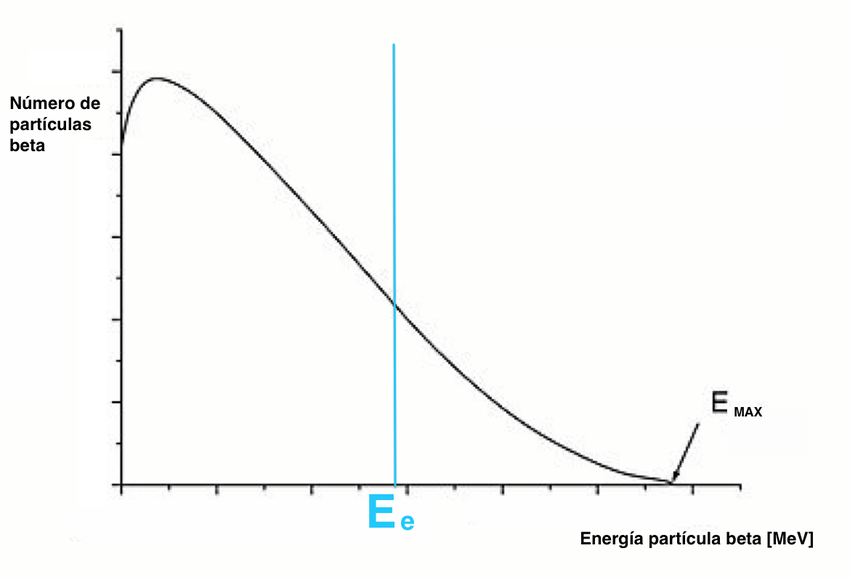
Y esto era un problema. Tal y como señaló Lise Meitner, si la transición observada era una desintegración del núcleo original (A,Z) a otro núcleo (A,Z+1) y un electrón, se trataría de una desintegración a dos cuerpos, para la cual era bien sabido que las leyes de conservación de la energía y el momento lineal implicaban una energía fija bien determinada para el electrón. Por lo tanto, el espectro continuo en la desintegración beta no tenía ningún sentido. La propia Meitner planteó que tal vez los electrones radiaban parte de su energía al salir del intenso campo eléctrico del núcleo o al entrar al detector, lo cual explicaría que fueran detectados con energías diferentes pese a ser emitidos siempre con la misma. No obstante, un importante experimento llevado a cabo por Charles Drummond Ellis y William Wooster en 1927 descartó esta hipótesis utilizando para ello técnicas calorimétricas capaces de determinar la energía total emitida en la reacción. La conclusión era clara: los electrones producidos en la desintegración beta tienen un espectro continuo, y eso parecía atentar contra la mismísima ley de conservación de la energía.
La segunda cuestión tiene que ver con el espín de los núcleos involucrados…
Breve inciso: Una explicación clara sobre lo que es el espín daría para un artículo independiente, así que por el momento simplemente debemos tener presente que es un número propio de cada partícula. Protones y electrones tienen espín igual a ½, por lo que decimos que su espín es semientero. Otras partículas tienen espín igual a 0, 1, … y decimos que tienen espín entero. Los espines se suman, lo que sirve para determinar el espín de partículas compuestas a partir de los espines individuales de las partículas componentes. Por ejemplo, una partícula compuesta por dos partículas de espín semientero tendrá espín entero. Y ahora volvamos a nuestra historia...
Consideremos el ejemplo del Nitrógeno-14. En el modelo nuclear protón-electrón mencionado más arriba, este núcleo estaría formado por 14 protones y 7 electrones. Al estar formado de un número impar de partículas con espín semientero, 21 concretamente, ha de ser necesariamente un núcleo con espín semientero. Sin embargo, diversos experimentos señalaban que el núcleo de Nitrógeno-14 tenía espín entero. Era evidente que algo no acababa de encajar en dicho modelo nuclear.
Nos encontramos por lo tanto a finales de los años 20 y contamos con serios problemas para entender la desintegración beta. La primera de las dos cuestiones, la relativa al espectro continuo de los electrones, fue la que focalizó la mayor parte de la atención de los físicos del momento, dando lugar a varias explicaciones muy exóticas. La más famosa de ellas es la propuesta por Niels Bohr, quien propuso que la energía NO se conservaba en los procesos nucleares individuales, siendo su “aparente” conservación a escala macroscópica un efecto estadístico. Aunque Bohr nunca llegó a publicar esta idea, sí que la defendió en cartas a sus colegas, así como en varias conferencias y discusiones. Dado que en estos momentos se estaba desarrollando la sorprendente mecánica cuántica, no es del todo de extrañar que algunas personas pusieran en duda absolutamente todos los pilares de la física clásica. Otra hipótesis exótica fue la planteada por George Paget Thomson, quien propuso que los átomos individuales de una sustancia radiactiva eran diferentes, una idea que fue pronto abandonada dado que los ritmos de desintegración observados eran completamente universales.
Y en este contexto nace el neutrino. Es importante notar que la dificultad para entender el espectro continuo de los electrones se debe a que estamos asumiendo que se trata de una desintegración a dos cuerpos, en la que la conservación de la energía impone una energía fija para los electrones. Pero… ¿y si hubiera una tercera partícula que no somos capaces de detectar? En ese caso los electrones tendrían que compartir su energía con dicha partícula, en ocasiones cediendo más y en ocasiones menos, lo que provocaría precisamente un espectro continuo. Ésta fue la idea del austriaco Wolfgang Pauli, quien no pudiendo acudir personalmente a una conferencia celebrada en Tübingen (Alemania), decidió presentarla a través de una famosa carta a sus “colegas radiactivos”. En esta carta (enviada personalmente a Lise Meitner el 4 de diciembre de 1930), Pauli planteaba la existencia de una nueva partícula neutra, muy ligera y de espín ½, que estaba escapando indetectada en la desintegración beta. Esta partícula es el neutrino, que así hizo su entrada en la física de partículas (aunque el nombre de “neutrino” fue introducido por Edoardo Amaldi y popularizado por Enrico Fermi unos años después). Además, si los neutrinos son constituyentes del núcleo, como los protones y electrones, pueden ayudar a resolver el problema del espín nuclear, tal y como el propio Pauli destaca en su carta. No obstante, este detalle es anecdótico, puesto que hoy sabemos que en realidad ni electrones ni neutrinos son parte del núcleo y que el problema del espín de los núcleos se resuelve con la introducción del neutrón, una partícula descubierta en 1932 por Chadwick.
Y así nació el neutrino como partícula hipotética. ¿Pero existiría realmente? ¡Así es! Los neutrinos fueron descubiertos experimentalmente por Frederick Reines y Clyde Cowan en 1956. Desde entonces los neutrinos nos han dado muchas sorpresas y hoy en día siguen motivando numerosos artículos teóricos y sofisticados experimentos. Por lo tanto… ¡larga vida a los neutrinos!
Bibliografía:
– The idea of the neutrino, L. M. Brown, Physics Today 31, Vol. 9 (1978) 23.
– When energy conservation seems to fail: the prediction of the neutrino, F. Guerra et al, Sci & Educ. 23 (2014) 1339–1359.
– Neutrino. History of a unique particle, S. M. Bilenky, European Physical Journal H 38 (2013) 345-404 [arXiv:1210.3065].

Un comentario en “El nacimiento del neutrino”